 Kirthana Balachandran
Kirthana BalachandranLa primera terapia que utiliza la edición genética se ofrecerá en el NHS, lo que supondrá un “avance revolucionario” para los pacientes.
Se utilizará como posible cura para el trastorno sanguíneo conocido como beta talasemia.
Se extraerán las células madre que forman la sangre, se reprogramarán para corregir la afección y se devolverán al cuerpo del paciente.
Podría ahorrarles la necesidad de una transfusión de sangre cada tres a cinco semanas de por vida.
Las personas con beta talasemia tienen dificultades para producir suficiente hemoglobina, que es la proteína de los glóbulos rojos que transporta oxígeno por todo el cuerpo.
Es una enfermedad genética que se transmite de padres a hijos y es causada por defectos en las instrucciones del cuerpo para fabricar hemoglobina.
Puede dejar a las personas severamente cansadas, débiles y con falta de aliento y también reduce la expectativa de vida.
A Kirthana Balachandran, de 21 años, le diagnosticaron la enfermedad cuando tenía solo tres meses y sufre dolores musculares y de espalda y puede tener palpitaciones al caminar cuesta arriba.
“La idea de depender de transfusiones durante literalmente el resto de mi vida es desalentadora; me preocupa constantemente el futuro”, afirma.
La idea de la edición genética es que sólo es necesario hacerlo una vez.
Cómo funciona la edición genética
Se basa en una herramienta llamada Crispr, que ganó el Premio Nobel de Química en 2020. Es esencialmente un navegador conectado a un par de tijeras: una parte apunta a la sección correcta del ADN y la otra realiza la edición.
Se podría pensar que esta tecnología se utiliza para reparar el defecto genético, pero en realidad es más lindo que eso.
En cambio, se basa en el hecho de que el cuerpo produce diferentes tipos de hemoglobina antes y después del nacimiento.
Cuando todavía estamos en el útero, nuestros cuerpos utilizan la “hemoglobina fetal” para extraer oxígeno del torrente sanguíneo de nuestra madre.
Una vez que nacemos, se activa un interruptor genético y comenzamos a producir “hemoglobina adulta”.
Esencialmente, sólo la forma adulta de hemoglobina es la que se ve afectada por la beta talasemia.
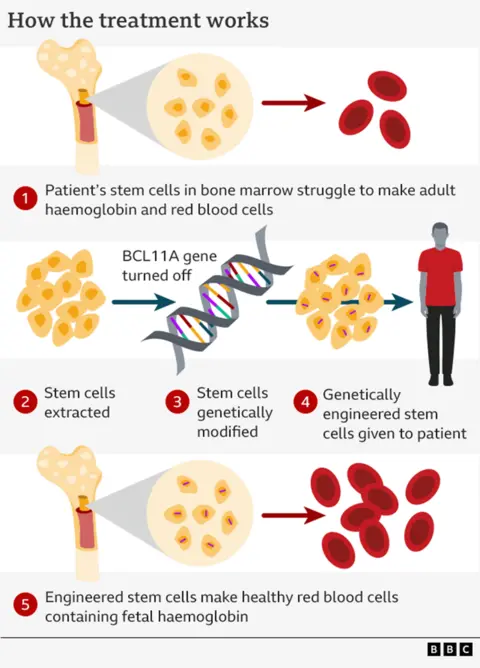
Entonces, la terapia desactiva el interruptor, llamado BCL11A, y el cuerpo adulto comienza a producir hemoglobina fetal nuevamente.
Para ello se extraen las células madre que fabrican los glóbulos rojos en nuestra médula ósea esponjosa.
Estas células se envían al laboratorio donde se activa el interruptor genético.
La siguiente etapa es desagradable. Se necesita un ciclo de quimioterapia para eliminar las células madre viejas que producían hemoglobina dañada, antes de poder introducir las nuevas.
Abdul-Qadeer Akhtar, de 28 años y de Hemel Hempstead, participó en ensayos clínicos en 2020.
Dijo que el tratamiento fue “desafiante” y “duro”, pero desde que lo recibió, ha estado “más saludable y más activo”.
“[I] “Incluso he empezado a boxear, ahora puedo viajar con más libertad, lo cual es fantástico, estoy ansioso por abrazar la vida al máximo”.
Los datos muestran De los 52 pacientes que recibieron el tratamiento, 49 no necesitaron otra transfusión sanguínea durante al menos un año de seguimiento. El enfoque es tan nuevo que aún se desconocen los efectos a largo plazo.
Kirthana dice: “Con la terapia genética, potencialmente podría curarme y no tendría que recibir mis transfusiones trimestrales.
“Sería un tratamiento que cambiaría mi vida”.
¿Un precio de 1,6 millones de libras?
El Instituto Nacional de Salud y Excelencia Asistencial, el organismo de control de medicamentos, aprobó la terapia después de evaluar los costos y beneficios de lo que llama una “cura potencial”.
Se ha llegado a un acuerdo que significa que NHS England pagará menos que el precio oficial de £ 1,6 millones por paciente.
Se estima que 460 personas mayores de 12 años serían elegibles si quisieran la terapia, y se ofrecerá en siete centros especializados “en unas semanas”.
Amanda Pritchard, directora ejecutiva del NHS, dijo: “Este es un momento histórico para las personas que viven con beta talasemia, ya que el NHS ahora ofrece una cura potencial para quienes enfrentan este trastorno debilitante”.
La beta talasemia afecta principalmente a personas de origen mediterráneo, del sur de Asia, del sudeste de Asia y de Oriente Medio.
Anteriormente, la única alternativa a las transfusiones de sangre era un trasplante de células madre, pero esto era poco común porque requería una compatibilidad muy cercana del tejido de un donante.
Casgevy, desarrollado por la empresa Vertex, es la primera terapia aprobada que utiliza la tecnología Crispr.
Romaine Maharaj, directora ejecutiva de la Sociedad de Talasemia del Reino Unido, dijo que “estamos al borde de un avance revolucionario” y “es un faro de esperanza”.
Todavía se están llevando a cabo negociaciones para ver si la misma terapia se puede utilizar en el NHS para otra enfermedad genética que afecta a la hemoglobina: la anemia de células falciformes.


